Sehr geehrte Kolleg*innen,
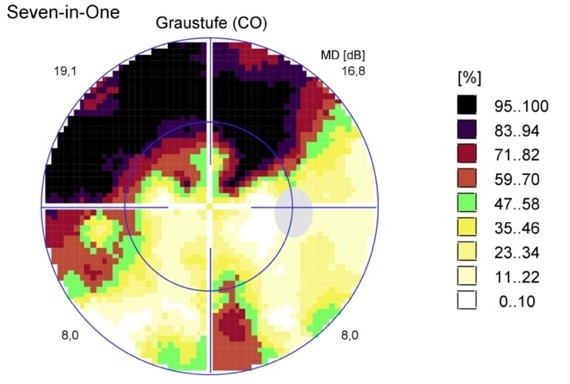
im Rahmen unserer von der DFG geförderten, multizentrischen VIRON-Studie wird ein erprobtes transorbitales Elektrostimulationsverfahren bei Patientinnen und Patienten mit manifesten Gesichtsfelddefekten aufgrund eines Primären Offenwinkelglaukoms untersucht. Ziel ist es, die bestehenden Gesichtsfelddefekte zu verkleinern und somit das Sehvermögen der Patientinnen und Patienten zu verbessern.
Insgesamt ist eine Behandlung von 300 Patientinnen und Patienten an den Universitätskliniken Bonn, Göttingen, Hamburg, Köln und Mainz vorgesehen.
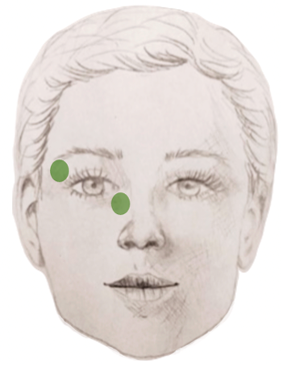
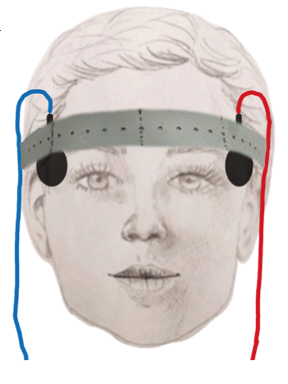
Die Patient*innen werden in drei Gruppen randomisiert:
(1) Gruppe 1 erhält eine klassische transorbitale Elektrostimulation über zwei im Bereich der Schläfen platzierte Elektroden.
(2) Für Gruppe 2 ist eine MRT-basierte, individualisiert an die Verteilung der periokulären Gewebe angepasste Elektrostimulation geplant.
(3) Patientinnen und Patienten der Gruppe 3 erhalten eine transorbitale Scheinstimulation.
Die Elektrostimulationsbehandlung wurde in mehreren Studien angewandt, um das Restsehen bei bestehender Optikusneuropathie zu reaktivieren. Die Behandlung verbesserte die Lichtdetektion und reduzierte die von den Patientinnen und Patienten berichteten Beeinträchtigungen des täglichen Lebens (Fedorov et al. 2011, Gall et al. 2013b, Gall et al. 2011, Gall et al. 2013c, Sabel et al. 2011a, Sabel et al. 2011b, Schmidt et al. 2013).
WELCHE RISIKEN SIND MIT DER BEHANDLUNG VERBUNDEN?
Die Behandlung ist erfahrungsgemäß für die Patientinnen und Patienten nicht oder allenfalls sehr geringfügig als leichtes Kribbeln auf der Kopfhaut oder in Form von Lichterscheinungen (sog. Phosphene, z.B. in Form von Blitzen) wahrnehmbar. Selten und lediglich nach kontinuierlicher Stromapplikation traten bei vorangegangenen Studien leichte Kopfschmerzen und Hautreizungen im Bereich der positionierten Elektroden auf, die relativ schnell vollständig reversibel waren (Antal et al. 2017).
WEN SUCHEN WIR?
Wir suchen Patient*innen zwischen dem 40. und 80. Lebensjahr, bei denen ein medikamentös stabil (nicht mehr als zwei verschiedene Sorten Augentropfen) eingestelltes Primäres Offenwinkelglaukom mit signifikanten Gesichtsfelddefekten (>5dB und <22dB) bekannt ist.
Für weitere Informationen (inkl. Ein- und Ausschlusskriterien) verweisen wir auf die Homepage des DRKS (Deutsches Register für klinische Studien):
WIE IST DER ABLAUF DER STUDIE?
Nach vier initialen Voruntersuchungen folgen insgesamt zehn Elektrostimulationsbehandlungen, die innerhalb von zwei Wochen werktäglich durchgeführt werden (die Wochenenden sind ausgenommen). Eine Stimulationsbehandlung dauert ca. 30 Minuten. Die Untersuchungs- und Behandlungstermine sind über einen Zeitraum von etwa sechs Wochen verteilt. Ein weiterer Untersuchungstermin findet nach sechs Monaten statt. Im Rahmen der Studie werden die folgenden Maßnahmen durchgeführt:
- Einwilligung zur Studienteilnahme
- Überprüfung der Ein- und Ausschlusskriterien
- Erhebung demographischer Daten, Ihrer Krankengeschichte (z.B. vorangegangene Operationen) und Dokumentation Ihrer Medikamente
- Bestimmung der Sehschärfe
- Augeninnendruckmessung
- Gesichtsfeldmessung
- Fragebögen zur Lebensqualität (SF-36) und der subjektiven Sehkraft (NEI VFQ-25)
- Untersuchungen der Netzhaut mittels Ganglienzell-OCT, RNFL und Fundusfoto
- MRT-Untersuchung für die randomisierte Gruppe
WAS MUSS BEI STUDIENTEILNAHME BEACHTEN WERDEN?
Um den geplanten Ablauf der Studie zu gewährleisten, ist es wichtig, dass alle vereinbarten Termine genau eingehalten werden.
KONTAKT
Sie haben geeignete Patient*innen, die Interesse haben, oder noch Fragen?
Dann melden Sie sich gerne per E-Mail oder Telefon an:
E-Mail:
Diese E-Mail-Adresse ist vor Spambots geschützt! Zur Anzeige muss JavaScript eingeschaltet sein! (für ärztliche Kolleginnen und Kollegen)
Diese E-Mail-Adresse ist vor Spambots geschützt! Zur Anzeige muss JavaScript eingeschaltet sein! (für Patientinnen und Patienten)
Telefon:
0551 – 39 64802

